3º Ano Ensino Médio - Noturno - Funções orgânicas Oxigenadas e nomenclatura (Ácido Carboxílico, Éster e Éter).
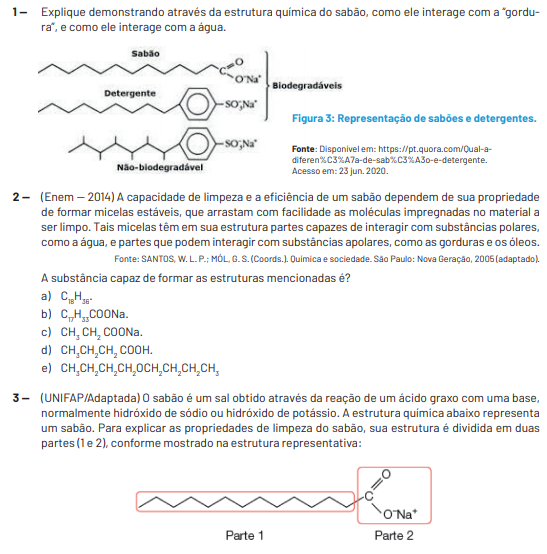
TEMA: Reação de Saponificação
TEXTO 1
TEXTO 1
HISTÓRIA DO SABONETE
Por Viviane Bigio
Muito provavelmente o homem fazia uso do sabonete desde a pré-história. Nem sabia da utilidade
que teria um dia para a humanidade.
Segundo uma lenda romana, a palavra “sabão” deriva da semelhança com Monte Sapo, nos arredores
de Roma, na Itália. A gordura dos animais que eram sacrificados no fogo para os deuses escorria na madeira queimada do altar até a proximidade dos rios onde as mulheres iam lavar roupas. E elas sentiam
certa facilidade em limpá-las com esta nova substância.
O nome “sabonete” teve origem na França, onde a palavra era Savon e onde introduziam nos sabonetes cores e aromas. Os sabões são resultado de uma reação química entre a gordura e um álcali (base
forte), resultando numa gordura de ação detergente. Na verdade o sabão foi inventado pelos fenícios
600 anos A.C. Eles ferviam a banha de cabra com água e cinzas de madeira, obtendo um sabão cremoso. Foi no século VII que os árabes descobriram o processo
de saponificação misturando óleos naturais, gordura animal e
soda cáustica. Esta mistura, depois de fervida, endurecia. Foi
quando surgiu o sabão sólido. Tendo aprendido com os árabes,
os espanhóis acrescentaram óleo de oliva a esta mistura para
dar-lhe um cheiro mais agradável.
Nos séculos XV e XVI várias cidades europeias se tornaram
produtoras de sabão. As mais conhecidas eram Marselha na
França e Savona na Itália, de onde foi originada a palavra Savon e o diminutivo Savonette ou sabonete. O sabão branco só
apareceu em 1978, ano que marcou o desenvolvimento do sabão moderno. Foi inventado o sabão branco depois da introdução acidental de ar na solução de sabão antes da moldagem.
Na época de Napoleão, na Europa, o banho ainda não era costume corrente. Muitas pessoas não o
praticavam. Até nos tempos da Rainha Elizabeth, acontecia eventualmente uma vez por ano. Felizmente, com o tempo este hábito tornou-se mais frequente ou até diário, mostrando como era importante a
remoção de microrganismos da pele, reduzindo os riscos de infecção da mesma. A introdução de fragrâncias aumentou o seu uso.
O uso medicinal dos sabões nos remete aos registros onde são mencionadas suas propriedades medicinais e de limpeza. Alguns cientistas usaram o sabão para curar certos problemas de pele, incluindo
a escabiose, a psoríase, a tinea e o herpes tonsurans. Na Europa, no século XIX foram descritos tratamentos com uso de sabonete para a acne e a micose. E nos EUA tentaram tratar a acne com sabão fino
feito de azeite de oliva e soda cáustica.
Com o ajuste das fórmulas e o desenvolvimento da indústria química, por volta dos anos 50 foi constatado um baixo índice de alergia ao uso de sabonete
como a diminuição de seu custo. Sua função é de eliminar pequenas partículas sólidas da pele, diminuindo o seu ressecamento. Podem também acrescentar óleos vegetais ou minerais.
A falta de glicerina nos sabonetes comerciais é
a principal razão de ressecamento na pele. Esta é a
principal diferença entre os sabonetes comerciais e
os sabonetes artesanais. Os ácidos graxos usados
nos sabonetes artesanais ajudam a regular a umidade e nutrir a pele, enquanto a glicerina natural dá
uma textura mais macia. Tomar um bom banho com
um sabonete cheiroso e macio é uma delícia.
(Texto retirado de: https://www.pucsp.br/maturidades/curiosidades/
curiosidades_ed62.html. Acesso em: 02 jul. de 2020).
Conceitos Básicos
A reação de saponificação é aquela em que um éster reage em meio aquoso com uma base forte,
ou seja, é uma hidrólise alcalina. Os produtos formados são um sal orgânico e um álcool. Essas reações
são denominadas de reações de saponificação porque, quando ocorre uma reação desse tipo, com um
triéster proveniente de ácidos graxos, formam-se os sabões.
Os ácidos graxos são ácidos carboxílicos de cadeia longa, em geral com 12 átomos de carbono ou
mais. Eles reagem com a glicerina (glicerol ou propanotriol), formando os glicerídeos, também denominados de triglicerídeos ou triacilgliceróis, que compõem os óleos e gorduras animais e vegetais:
Assim, o sabão é produzido por meio do aquecimento de óleos ou gorduras vegetais em uma solução aquosa de uma base forte, como o hidróxido de sódio, que é conhecido comercialmente por
soda cáustica.
O sabão formado possui em sua estrutura uma longa cadeia proveniente do ácido graxo que constitui uma parte apolar, enquanto sua extremidade é polar. Isso permite que a parte apolar interaja com as
sujeiras gordurosas que também são apolares, enquanto a extremidade polar interage com a água, que
também é polar. É assim que os sabões conseguem diminuir a tensão superficial da água (por isso são
também chamados de agentes tensoativos ou de surfactantes), eliminando a sujeira.
Fonte: Manual da Química: Reação de Saponificação: Disponível em:
https://www.manualdaquimica.com/quimica-organica/reacao-saponificacao.htm. Acesso em: 19 jun. 2020.
ATIVIDADES



Comentários
Postar um comentário